为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: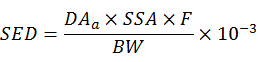 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: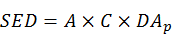 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: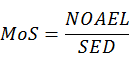 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):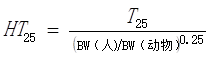 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。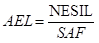 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: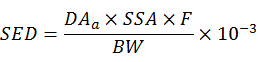 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: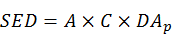 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: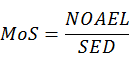 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):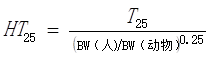 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。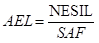 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: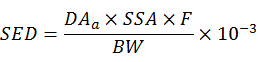 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: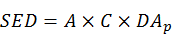 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: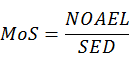 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):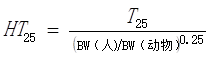 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。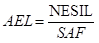 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: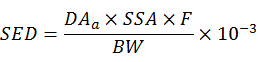 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: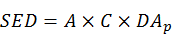 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: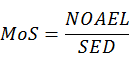 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):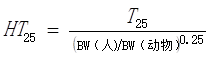 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。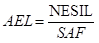 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: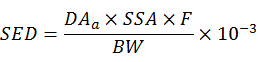 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: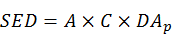 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: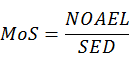 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):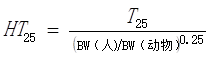 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。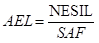 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: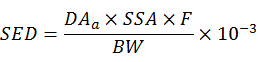 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: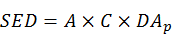 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: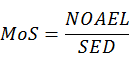 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):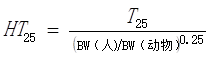 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。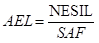 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: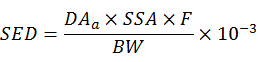 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: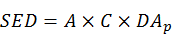 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: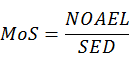 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):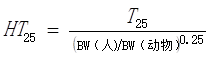 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。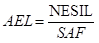 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: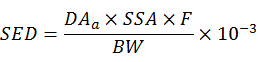 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: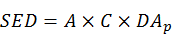 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: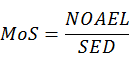 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):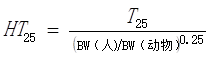 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。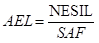 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》
为保障化妆品使用安全,规范化妆品安全评估,指导开展相关工作,制定本导则。
1.适用范围
本导则适用于化妆品原料和产品的安全评估。
2.基本原则与要求
2.1原料的安全性是化妆品产品安全的前提条件。化妆品原料的风险评估包括原料本身及可能带入的风险物质;化妆品产品一般可认为是各种原料的组合,应基于所有原料和风险物质进行评估,如果确认某些原料之间存在化学和/或生物学等相互作用的,应该对其产生的风险物质进行评估。
2.2化妆品安全评估应以现有科学数据和相关信息为基础,遵循科学、公正、透明和个案分析的原则,在实施过程中应保证安全评估工作的独立性。
2.3化妆品安全评估引用的参考资料应为全文形式公开发表的技术报告、通告、专业书籍或学术论文,以及国际权威机构发布的数据或风险评估资料等;应用未公开发表的研究结果时,需经数据所有权方授权,并分析结果的科学性、准确性和可靠性等。
2.4化妆品的安全评估工作由具有相应能力的安全评估人员按照本导则的要求进行评估,并出具评估报告。
2.5化妆品注册人、备案人应自行或委托专业机构开展安全评估。
2.6化妆品的安全评估资料根据需要应当及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
2.7化妆品安全评估报告结论不足以排除产品对人体健康存在风险的,应当采用毒理学试验方法进行产品安全性评价。
2.8化妆品安全评估人员开展安全评估时,以本导则作为参考依据,还应根据原料和产品的具体情况进行分析。
2.9评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
3.化妆品安全评估人员的要求
化妆品安全评估人员应符合以下要求:
3.1具有医学、药学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
3.2能够查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3.3能够公平、客观的分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作。
3.4能定期接受相应的专业培训,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。
4.风险评估程序
化妆品原料和风险物质的风险评估程序分为以下四个步骤:
4.1危害识别
基于毒理学试验、临床研究、不良反应监测和人群流行病学研究等的结果,从原料和风险物质的物理、化学和毒理学特征来确定其是否对人体健康存在潜在危害。
4.1.1健康危害效应
根据产品的使用方法、暴露途径等,确认原料和风险物质可能存在的健康危害效应,主要包括:
(1)急性毒性:包括经口和经皮后产生的急性毒性效应。
(2)刺激性/腐蚀性:包括皮肤和眼刺激性/腐蚀性效应。
(3)致敏性:主要为皮肤致敏性。
(4)光毒性:紫外线照射后产生的光刺激性。
(5)光变态反应:重复接触并在紫外线照射下引起的皮肤反应。
(6)致突变性:包括基因突变和染色体畸变效应等。
(7)重复剂量毒性:连续暴露后对组织和靶器官所产生的功能性和/或器质性改变。
(8)致畸性:在胚胎发育期引起胎仔永久性结构和功能异常的作用。
(9)生殖和发育毒性:对亲代的生殖功能及对子代发育过程的有害作用。
(10)慢性毒性/致癌性:正常生命周期大部分时间暴露后所产生的毒性效应及引起肿瘤的可能性。
(11)其他:有吸入暴露可能时,需考虑吸入暴露引起的健康危害效应。
4.1.2危害识别
(1)按照我国现行的《化妆品安全技术规范》(以下简称《规范》)或国际上通用的毒理学试验结果的判定原则对化妆品原料和风险物质的急性毒性、皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、致敏性、光毒性、光变态反应、致突变性、重复剂量毒性、致畸性、生殖和发育毒性、慢性毒性/致癌性等毒性特征进行判定,确定原料和风险物质的主要毒性特征及程度。
(2)根据所提供的化妆品原料和风险物质的人群流行病学调查、人群监测以及临床不良事件报告等相关资料,判定该原料和风险物质可能对人体产生的健康危害效应。
(3)在对危害识别进行判定时,还应考虑到原料的纯度和稳定性、其可能与终产品中其它组分发生的反应以及透皮吸收的能力等,同时还应考虑到原料和生产过程中不可避免带入的风险物质的健康危害效应等。
(4)对可能有吸入暴露风险的产品,如喷雾产品,应评估其吸入暴露对人体可能产生的健康危害效应。
(5)对于复配原料,应对原料本身和/或每种组分的危害效应进行识别。
4.2剂量反应关系评估
用于确定原料和风险物质的毒性反应与暴露剂量之间的关系。对有阈值效应的原料和风险物质,需获得未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL),如果不能得到NOAEL的,则采用其观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)。但用LOAEL值计算安全边际值(Margin of Safety,MoS)时,应增加相应的不确定因子(一般为3倍)。对于无阈值的致癌物而言,用剂量描述参数T25等来确定。对于具有潜在致敏风险的原料和风险物质,还需通过预期无诱导致敏剂量(No Expected Sensitization Induction Level,NESIL)来评估其致敏性。
4.2.1有阈值原料的剂量反应关系评估,需确定原料的NOAEL值。
当选择NOAEL计算安全系数时,应选择来自重复剂量毒性试验的数据,如90天经口毒性试验、慢性毒性/致癌试验、致畸试验、生殖和发育毒性试验等,还应该考虑该值获得的试验条件与被评估物质使用条件和品种敏感度的相关性。如果选择28天经口毒性试验数据时,应增加相应的不确定因子(一般为3倍)。
也可用基准剂量(Benchmark Dose,BMD)值进行安全评估。
4.2.2对于无阈值原料的致癌性,可通过剂量描述参数T25等来进行剂量反应关系评估。
4.2.3对于可能存在致敏风险的原料或风险物质,可通过NESIL进行安全评估。
4.3暴露评估
指通过对化妆品原料和风险物质暴露于人体的部位、浓度、频率以及持续时间等的评估,确定其暴露水平。
4.3.1进行暴露评估时,应考虑含该原料或风险物质产品的使用部位、使用量、浓度、使用频率以及持续时间等因素,具体包括:
(1)用于化妆品中的类别。
(2)暴露部位或途径:皮肤、粘膜暴露,以及可能的吸入暴露。
(3)暴露频率:包括间隔使用或每天使用的次数等。
(4)暴露持续时间:包括驻留或用后清洗等。
(5)暴露量:包括每次使用量及每日使用总量等。
(6)浓度:在产品中的浓度。
(7)透皮吸收率。
(8)暴露对象的特殊性:如儿童、孕妇、哺乳期妇女等。
4.3.2全身暴露量(Systemic Exposure Dosage,SED)的计算
(1)如果暴露是以每次使用经皮吸收μg/cm2时,根据使用面积,按以下公式计算: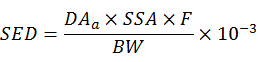 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
DAa:经皮吸收量(μg/cm2),每平方厘米所吸收的原料或风险物质的量,测试条件应该和产品的实际使用条件一致
SSA:暴露于化妆品的皮肤表面积(cm2)
F:产品的日使用次数(day-1)
BW:默认的人体体重(60kg)
(2)如果经皮吸收率是以百分比形式给予时,根据使用量,按以下公式计算: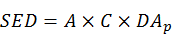 其中:
其中:
SED:全身暴露量(mg/kg•bw/day)
A:以单位体重计的化妆品每天使用量(mg/kg•bw/day)
C:在产品中的浓度(%)
DAp:经皮吸收率(%)。在无透皮吸收数据时,吸收率以100%计;若当原料分子量﹥500道尔顿,高度电离,且脂水分配系数Log Pow≤-1或≥4,熔点>200℃时,吸收率取10%。吸收率不以100%计时,需提供有关情况说明。
暴露量计算时还应考虑其他暴露途径的可能性(如吸入、食用等);必要时应考虑除化妆品外其他可能来源(如:食品和环境等)的暴露情况。
4.4风险特征描述
指化妆品原料和风险物质对人体健康造成损害的可能性和损害程度。可通过计算安全边际值、剂量描述参数T25、国际公认的致癌评估导则或预期无诱导致敏剂量等方式进行描述。
4.4.1有阈值原料和风险物质的风险特征描述
对于有阈值的化合物,通常通过计算其安全边际进行评估。计算公式为: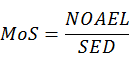 其中:
其中:
MoS:安全边际
NOAEL:未观察到有害作用的剂量
SED:全身暴露量(mg/kg•bw/day)
在通常情况下,当MoS≥100时,可以判定是安全的。
如化妆品原料或风险物质的MoS<100,则认为其具有一定的风险性,原则上不允许使用。对于特殊使用方式的原料如染发剂,当MoS值小于100时,需进一步进行评估。
100是指默认的不确定因子(UF),由种间差异10和种内差异10相乘所得,如有毒代动力学等数据,应考虑进行调整。如果毒理学数据质量存在缺陷,应适当增加不确定因子。
4.4.2无阈值原料的风险特征描述
对于无阈值的原料和风险物质,可通过计算其终生致癌风险度(Lifetime Cancer Risk,LCR)进行风险程度的评估。计算如下:
(1)首先按照以下公式将动物试验获得的T25转换成人T25(HT25):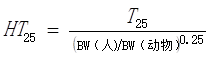 式中:
式中:
T25:对自发肿瘤发生率进行校正后,25%的实验动物的某部位有发生肿瘤的剂量。
HT25:由T25转换的人T25
BW:体重kg(默认的成人体重为60kg)
(2)根据计算得出的HT25以及暴露量按以下公式计算终生致癌风险: 式中:
式中:
LCR:终生致癌风险
SED:终生每日暴露平均剂量(mg/kg•bw/day)
如果该原料或风险物质的终生致癌风险度<10-6,则认为其引起癌症的风险性较低,可以安全使用。
如果该原料或风险物质的终生致癌风险度≥10-6,则认为其引起癌症的风险性较高,应对其使用的安全性予以关注。
4.4.3致敏性风险特征描述
对于潜在致敏风险的原料和风险物质,可按以下公式通过预期无诱导致敏剂量计算得出AEL。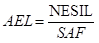 式中:
式中:
AEL:可接受暴露水平(μg/cm2)
NESIL:预期无诱导致敏剂量(μg/cm2)
SAF:致敏评估因子,根据个体差异、产品类型、使用部位、使用频率/持续时间等,确定恰当的致敏评估因子。
当AEL低于消费者暴露水平时,认为其引起致敏性的风险较高,应对其使用的安全性予以关注。
5.毒理学研究
通过一系列毒理学试验,测定化妆品原料和风险物质的毒理学情况,将其作为危害识别的一部分,也是化妆品安全评估的基础。毒理学试验首选《规范》收录的方法,选用其他国内外权威机构发布的毒理学试验方法时,应提供所采用方法的来源、与《规范》中方法相关性等信息。
5.1急性毒性
包括急性经口和/或经皮试验等。急性毒性试验可提供短时间染毒对健康危害的信息。试验结果可作为化妆品原料和风险物质毒性分级和标签标识以及确定重复毒性试验和其它毒理学试验剂量的依据。
5.2刺激性/腐蚀性
包括皮肤和/或眼睛的刺激性/腐蚀性试验。确定和评价原料和风险物质对皮肤局部或眼睛是否有刺激作用或腐蚀作用及其程度。
5.3皮肤致敏性
皮肤变态反应试验确定重复接触化妆品原料和风险物质是否可引起变态反应及其程度。
5.4皮肤光毒性
皮肤光毒性试验评价化妆品原料和风险物质引起皮肤光毒性的可能性。
5.5皮肤光变态反应
皮肤光变态反应试验可评估重复接触化妆品原料和风险物质,并在紫外照射下引起皮肤光变态反应的可能性。
5.6致突变性/遗传毒性
评价化妆品原料和风险物质引起遗传毒性的可能性,至少应包括一项基因突变试验和一项染色体畸变试验资料。
5.7重复剂量毒性
包括重复剂量经口和/或经皮毒性试验。
通过重复剂量经口毒性试验不仅可获得一定时期内反复接触受试物后引起的健康效应、受试物作用靶器官和受试物体内蓄积能力资料,并可估计接触的无有害作用水平,后者可用于选择和确定慢性试验的接触水平和初步计算人群接触的安全性水平。
通过重复剂量经皮毒性试验不仅可获得在一定时期内反复接触受试物后可能引起的健康影响资料,而且为评价受试物经皮渗透性、作用靶器官和慢性皮肤毒性试验剂量选择提供依据。
5.8致畸性:致畸试验用于检测妊娠动物接触化妆品原料和风险物质后引起胎鼠畸形的可能性。
5.9生殖和发育毒性
生殖和发育毒性检测妊娠动物接触化妆品原料和风险物质后引起子代发育异常和亲代生殖功能损害的可能性。
5.10慢性毒性/致癌性
慢性毒性试验是使动物长期地以一定方式接触受试物而引起毒性反应的试验。当某种化学物质经短期筛选试验预测具有潜在致癌性,或其化学结构与某种已知致癌剂十分相近时,需用致癌性试验进一步验证。
5.11毒代动力学
毒代动力学试验是定量地研究在毒性剂量下原料和风险物质在动物体内的吸收、分布、代谢、排泄过程和特点,进而探讨其毒性的发生和发展的规律,了解其在动物体内的分布及其靶器官。同时了解不同物种在动力学方面的差异可以为从动物实验结果外推到人时的不确定因子(UF)提供理论支持。
原料和风险物质经过皮肤吸收后,其代谢转化可能会对其潜在毒性、体内分布和排泄造成重要影响。因此,在特定情况下,需要实施体内或体外生物转化研究,以证明或排除某些不良反应。
5.12透皮吸收
原料和风险物质的透皮吸收试验,可采用国际通用的透皮吸收试验方法获取相应的数据。重均分子量大于1000道尔顿,且分子量小于1000道尔顿的低聚体含量少于10%,结构和性质稳定的聚合物,可不考虑透皮吸收。
5.13其它毒理学试验资料:有经呼吸道吸收可能时,需提供吸入毒性试验资料;必要时可提供其它有助于表明原料和风险物质毒性的毒理学试验资料。
5.14人群安全性试验资料
包括人体安全性试验资料和人群流行病学资料。
人群流行病学资料包括人群流行病学调查、人群监测以及临床不良事件报告、事故报告等。
6.化妆品原料的风险评估
6.1风险评估原则
6.1.1按照风险评估程序对化妆品原料和其可能存在的风险物质进行风险评估,保障原料使用的安全性。
6.1.2使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料应满足规范要求。
6.1.3凡国际权威化妆品安全评估机构已公布评估结论的原料,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.4凡世界卫生组织(WHO)、联合国粮农组织(FAO)、经济合作与发展组织(OECD)等权威机构已公布安全限量(如:每日允许摄入量(Acceptable Daily Intake,ADI)、每日耐受剂量(Tolerable Daily Intake,TDI)、参考剂量(Reference Dose,RfD)等)或结论(如一般认为安全物质(GRAS)、具有悠久食用历史)的原料,需对相关资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关结论。如缺少局部毒性资料,需对其局部毒性另行进行风险评估。如不同的权威机构评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
6.1.5如香精符合国际日用香料协会(IFRA)标准,需对相关评估资料进行分析,在符合我国化妆品相关法规规定的情况下,可采用相关评估结论。
6.1.6对于化学结构明确,且不包含致癌警告结构的原料或风险物质,含量较低且缺乏系统毒理学研究数据时,可参考使用毒理学关注阈值(Threshold of Toxicological Concern,TTC)等方法进行风险评价,但该方法不适用于金属或金属化合物、强致癌物(如黄曲霉毒素、亚硝基化合物、联苯胺类和肼等)、蛋白质、类固醇、高分子质量的物质、有很强生物蓄积性物质以及放射性化学物质和化学结构未知的化学混合物等。
6.1.7对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行风险评估。所参照的化学物与该原料或风险物质有相似的化学结构,相同的代谢途径和化学/生物反应性,其中结构相似性表现在:①各化学物质具有相同的官能团(如醛类、环氧化物、酯类、特殊金属离子物质);②各化学物质具有相同的组分或被归为相同的危害级别,具有相似的碳链长度;③各化学物质在结构上(如碳链长度)呈现递增或保持不变的特征,这种特征可以通过观察各化学物质的理化特性得到;④各化学物质由于结构的相似性,通过化学物质或生物作用后,具有相同的前驱体或降解产物可能性。
6.1.8根据原料理化特性、定量构效关系、毒理学资料、使用历史、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,可增加或减免毒理学终点的评估。
6.2化妆品原料的理化性质
原料的理化性质可用于预测特定的毒理学特性。根据产品配方,逐一掌握所用原料的理化性质信息。一般包括以下内容:
6.2.1原料的名称
包括通用名称、商品名称、INCI名称、标准中文名称、CAS号、EINCES号等。
6.2.2物理状态
如固体、液体、挥发性气体等。
6.2.3分子结构式和相对分子量
对于复配原料,必须说明每个组成成分的分子结构式和相对分子量。
6.2.4化学特性和纯度
应说明表征化学特性时使用的技术条件(紫外光谱或红外光谱、核磁、质谱、元素分析等)以及检测结果等。
应明确原料的纯度以及测定方法,并验证分析方法的有效性。
在理化试验和毒性试验中使用的原料必须与终产品中使用的原料质量规格相同。
6.2.5杂质/残留物
除了物质的纯度以外,还必须说明可能存在的杂质/残留物的浓度或含量。
6.2.6溶解度
应说明原料在水中和/或任何其他相关有机溶剂的溶解度。
6.2.7分配系数(Log Pow)
应说明分配系数。对于其计算值,应说明计算方法。
6.2.8其他相关的理化指标
如对于可吸收紫外线的成分,应说明化合物的紫外线吸收的波长及紫外线吸收光谱。
6.2.9均质性和稳定性
应说明试验条件下检测原料时使用的试验溶液的均质性。
应说明试验条件下原料的稳定性和储存条件。
6.2.10 UV-VIS吸收光谱
基于原料的结构,应提供UV-VIS吸收光谱。
6.2.11异构体组成
原料存在异构体时,各相关异构体也应进行风险评估。
6.2.12功能和用途
该原料拟用或已用于化妆品中的使用目的、化妆品中的最高浓度等。如果化妆品原料用于喷雾产品,应该明确提及吸入暴露的可能,并且应考虑吸入暴露的健康危害效应。
此外,此原料作为其他用途(例如消费产品,工业产品)时,所用浓度也应尽可能描述。
6.3矿物、动物、植物、生物技术来源的原料
6.3.1.矿物来源的原料,应包括以下内容:
(1)原料来源;
(2)制备工艺:物理加工、化学修饰、纯化方法及净化方法等;
(3)特征性组成要素:特征性成分(%);
(4)组成成分的理化特性;
(5)微生物情况;
(6)防腐剂和/或其它添加剂。
6.3.2动物来源的原料,应包括以下内容:
(1)物种来源(牛、羊、甲壳动物等)、物种通用名称、种属名称包括物种、属、科及使用的器官组织(胎盘、血清、软骨等);
(2)原产国;
(3)制备过程:萃取条件、水解类型、纯化方法等;
(4)特征性成分含量;
(5)形态:粉末、溶液、悬浮液等;
(6)特征性组成要素:特征性的氨基酸、总氮、多糖等;
(7)理化特性;
(8)微生物情况(包括病毒性污染);
(9)防腐剂和/或其它添加剂。
6.3.3植物来源的原料,应包括以下信息:
(1)植物的通用名称;
(2)种属名称包括物种、属、科;
(3)所用植物的部分;
(4)感官描述:粉末、液态、色彩、气味等;
(5)形态解剖学描述;
(6)自然生态和地理分布;
(7)植物的来源包括地理来源以及是否栽培或野生;
(8)具体制备过程:收集、洗涤、干燥、萃取等;
(9)储存条件;
(10)特征性组成要素:特征性成分;
(11)理化特性;
(12)微生物情况包括真菌感染;
(13)农药、重金属残留等;
(14)防腐剂和/或其它添加剂;
(15)如果是提取液,应说明包含的溶剂和有效成分的含量。
6.3.4生物技术来源的原料,应包括以下内容:
(1)制备过程;
(2)所用的生物描述:供体生物、受体生物、修饰微生物;
(3)宿主致病性;
(4)毒性成分包括生物代谢物、产生的毒素等;
(5)理化特性;
(6)微生物质量控制措施;
(7)防腐剂和/或其它添加剂。
对于特殊生物技术来源的原料,其中经修饰的微生物或潜在的毒性物质不能彻底去除的,需提供数据予以说明。
6.4香精香料
香精香料应符合我国相关国家标准或国际日用香料协会(IFRA)标准,此外,还应包括以下内容:
6.4.1天然来源的成分在香料混合物中的半定量浓度(即,<0.1%;0.1%至<1%,1%至<5%,5%至<10%,10%至<20%,20%及以上)。
6.4.2对于天然原料,应具有以下信息
(1)该批次天然原料的组分分析;
(2)天然原料中组分的最高含量水平,应考虑到批间差异;
(3)应明确说明使用了最大浓度化合物的化妆品类型。
7.化妆品产品的安全评估
7.1评价原则
7.1.1化妆品产品的安全评估应以暴露为导向,结合产品的使用方式、使用部位、使用量、残留等暴露水平,对化妆品产品进行安全评估,以确保产品安全性。
7.1.2按照4.风险评估程序对化妆品中的各原料和风险物质进行风险评估。使用《规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料、有限制要求的风险物质应满足规范要求;国外权威机构已建立相关限量值或已有相关评估结论的原料和风险物质,可采用其风险评估结论,如不同的权威机构的限量值或评估结果不一致时,根据数据的可靠性和相关性,科学合理的采用相关评估结论。
7.1.3完成化妆品产品的安全评估后,可以在满足伦理要求的前提下,通过人体皮肤斑贴试验或人体试用试验,进一步排除化妆品产品的皮肤不良反应。
7.1.4配方相似、种类相同,且系列名称相同产品,在配方之间的差异不影响产品安全性的前提下,可以参考已有的资料和数据,只对调整组分进行评估。
7.1.5如果产品配方中两种或两种以上的原料,其可能产生系统毒性的作用机制相同,必要时应考虑原料的累积暴露,并进行具体的个案分析。
7.1.6如果产品中所含原料还可能来源于除该类化妆品外的其他产品,如:化妆品、食品、环境等时,在计算安全边际时应考虑累积暴露,并进行具体分析。
7.1.7应针对每个产品编写安全评估报告,妥善保存,及时补充上市后的安全资料。
7.2产品理化稳定性评价
7.2.1对于上市的每个批次的化妆品产品,应结合产品的具体情况评价相关理化指标,一般包括以下参数:
(1)物理状态;
(2)剂型(乳液、粉等);
(3)感官特性(颜色、气味等);
(4)pH值(在...℃条件下);
(5)粘度(在...℃条件下);
(6)根据具体需要的其他方面。
7.2.2确认原料之间是否存在化学和/或生物学相互作用,并考虑相互作用产生的潜在安全风险。如存在潜在安全风险的,应当结合相关文献研究资料或理化实验数据,进行风险评估。
7.2.3对与内容物接触容器或载体的物理稳定性以及与产品的相容性进行风险评估。
可参考包装或载体供应商的安全资料或安全声明等资料,对容器的稳定性进行风险评估。
7.2.4对配方体系近似,包装材质相同的化妆品,可根据已有的资料和实验数据对理化稳定性开展风险评估工作,但需阐明理由,说明情况。
7.3产品微生物学评估
7.3.1化妆品微生物污染通常来源于原料带入,产品制备和灌装过程,以及消费者使用环节。儿童用化妆品、眼部/口唇化妆品,应当对微生物污染予以特别关注。
7.3.2对于正在研发中的化妆品,可按照化妆品防腐效能评价方法操作程序(见附录3)对其防腐体系的有效性进行评价。
7.3.3对于防腐体系相同且配方近似的产品,可参考已有的资料和实验数据进行产品安全性评价。根据产品特性,属于不易受微生物污染的产品,如乙醇含量>20%(体积)、以有机溶剂为主、高/低pH值(≥10或≤3)、一次性或包装不能开启等类型的产品,可不进行微生物挑战试验,但化妆品安全性评估人员应就相关情况予以说明。
7.4产品上市后的安全监测
7.4.1对上市后产品的安全性进行监测、记录和归档。包括正常使用和不当使用时发生的不良反应,消费者投诉以及后续随访等。
7.4.2如上市产品出现下列情况,需重新评估产品的安全性:
(1)上市产品所用原料在毒理学上有新的发现,且会影响现有风险评估结果的;
(2)上市产品的原料质量规格发生足以引起现有风险评估结果变化的;
(3)上市产品不良反应出现连续、呈明显增加趋势,或出现了严重不良反应的;
(4)其他影响产品质量安全的情况。
7.5儿童化妆品评估要求
7.5.1进行儿童化妆品评估时,在危害识别、暴露量计算等方面,应结合儿童生理特点。
7.5.2应明确其配方设计的原则,并对配方使用原料的必要性进行说明,特别是香精、着色剂、防腐剂及表面活性剂等原料。
7.5.3原则上不允许使用以祛斑美白、祛痘、脱毛、除臭、去屑、防脱发、染发、烫发为目的的功效成分,如因其他目的使用时,需对其使用的必要性及针对儿童产品使用的安全性进行评价。
7.5.4应选用有一定安全使用历史的化妆品原料,不鼓励使用基因技术、纳米技术等新技术制备的原料,如无替代原料必须使用时,需说明原因,并针对儿童产品使用的安全性进行评价。
8.安全评估报告
8.1化妆品原料的风险评估报告
化妆品原料的风险评估报告,其通常包括摘要、原料理化性质、风险评估过程、风险评估结果分析、风险控制措施或建议、风险评估结论、证明性资料、评估人员签名及资质证明等内容。
参考格式详见附录1。
8.2化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括安全评估摘要、产品简介、产品配方、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。
参考格式详见附录2。
9.说明
本导则所列条款为化妆品安全评估中所涉及的全部内容,具体进行产品的评估时,评估人员需参照本导则结合产品的实际情况进行评估。
10.术语和释义
下列术语和释义适用于本导则。
10.1危害(Hazard)
原料或风险物质在暴露情况下对人体产生不良影响的属性。
10.2风险(Risk)
暴露条件下,原料或风险物质对使用者产生有害作用的可能性及强度的定量和定性估计。
10.3剂量(Dose)
直接与机体的吸收部位(消化道、粘膜、皮肤等)接触,可供吸收的量,通常以mg/kg•bw表示。
10.4未观察到有害作用的剂量(No Observed Adverse Effect Level,NOAEL)
在规定的试验条件下,用现有的技术手段或检测指标未观察到任何与受试物有关的毒性作用的最大剂量。
10.5观察到有害作用的最低剂量(Lowest Observed Adverse Effect Level,LOAEL)
在规定的试验条件下,受试物引起实验动物组织形态、功能、生长发育等有害效应的最低剂量。
10.6基准剂量(Benchmark Dose,BMD)
一种物质引起某种特定的、较低健康风险发生率(一般在1%~10%之间)的剂量。
10.7有阈值化学物质(Threshold Compounds)
在一定的暴露剂量以下,对动物或人不发生有害作用的化学物质,包括非致癌物和非遗传毒性的致癌物。
10.8无阈值化学物质(Non-Threshold Compounds)
多为遗传毒性的致癌物,是已知或假设其作用是无阈值的,即已知或假设大于零的所有剂量都可以诱导出有害作用的化合物。
10.9全身暴露量(Systemic Exposure Dosage,SED)
通过各种暴露途径进入体循环的化学物质的预计量。通常以mg/kg•bw/day表示。
10.10安全边际(Margin of Safety,MoS)
从重复剂量毒性试验得到的NOAEL与预期的全身暴露量之间的比值。
10.11致癌的可接受风险度(Acceptable Risk of Cancer)
能够为社会公认并能为公众接受的终生致癌风险概率,通常应小于10-6,可因时间、地点、条件和公众的接受能力而不同。
10.12 T25
对自发肿瘤发生率进行校正后,引起25%的实验动物出现肿瘤的剂量。
10.13每日允许摄入量(Acceptable Daily Intake,ADI)
是指人终生每日从食物或饮水中摄入某种化学物质,对健康无任何已知不良效应的剂量。
10.14每日耐受剂量(Tolerable Daily Intake,TDI)
是指人终生每日摄入某种物质,对健康无任何已知不良效应的剂量。
10.15参考剂量(Reference Dose,RfD)
环境介质(空气、水、土壤、食品等)中化学物质的日平均接触剂量的估计值,人群(包括敏感亚群)在终生接触该剂量水平下,预期一生中发生非致癌或非致突变有害效应的危险度可接受或可忽略。
10.16预期无诱导皮肤过敏的剂量水平(No Expected Sensitization Induction Level,简称:NESIL)
不产生诱导致敏效应的最高剂量或浓度。
10.17毒理学关注阈值(Threshold of Toxicological Concern,TTC)
化学品暴露阈值,在该暴露水平下,预计不存在危害人类健康的风险。
附录1
化妆品产品的安全评估报告 题目:(原料名称)安全评估报告 公司名称:************************ 公司地址:************************ 评估单位:************************ 评估人:************************ 评估日期:********年*****月*****日 一、安全评估摘要:
**为**(使用方法、剂型等)产品,使用目的**,依据《化妆品安全评估导则》,对产品中的**、**(具体原料名称),**、**(具体风险物质名称)进行安全评估,以及……(其他安全资料)。结果显示,该产品在正常、合理及可预见的使用情况下不会对人体健康造成危害。
二、产品简介:
1.产品名称:配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录
2.产品使用目的及使用方式
3.日均使用量(g/day):
4.驻留因子:
5.其他:
三、产品配方
四、配方设计原则(仅针对儿童化妆品)
五、配方中各成分的安全评估:
1.危害识别:
一般包括:
(1)急性毒性
(2)刺激性/腐蚀性
(3)皮肤致敏性
(4)皮肤光毒性
(5)光变态反应
(6)致突变性/遗传毒性
(7)重复剂量毒性
(8)发育和生殖毒性
(9)慢性毒性/致癌性
(10)毒代动力学
(11)人群安全资料
2.剂量反应关系评估:
3.暴露评估:
4.风险特征描述:
六、可能存在的风险物质评估
七、风险控制措施或建议:(如警示用语、使用方法)
八、安全评估结论:(一般包括产品理化稳定性评估结论;产品微生物稳定性评估结论;人体安全数据,包括:临床数据、消费者使用调查、不良反应记录等。检测结论,各原料的评估结论)
九、安全评估人员签名
十、安全评估人员资质证明(简历)
十一、参考文献
十二、附录,包括检测报告、涉及的原料质量规格证明等。
附录3
化妆品安全评估操作实施指南 为保障化妆品质量安全,做好化妆品安全评估工作,促进行业安全评估能力稳步提升,根据《化妆品监督管理条例》和《化妆品安全评估技术导则》等有关规定,结合化妆品行业现状,制定此操作指南。
与欧美发达国家相比,我国化妆品行业整体安全评价水平还有差距,因此在过渡期内,《产品配方整体安全分析》(具体见示例1)可作为化妆品产品安全评估资料,用于保障化妆品的质量安全。
一、《产品配方整体安全分析》的主要内容
《产品配方整体安全分析》是根据《化妆品安全技术规范》(2015年版)、权威机构的评估结果、原料历史使用浓度、化妆品监管部门公布的原料最高历史使用量等不同证据类型,对产品配方进行分析以确定其安全性,在过渡期内可作为化妆品产品安全评估资料用于保障化妆品的质量安全。主要内容包括:
(一)摘要。
(二)产品简介。包括产品名称、使用方法、日均使用量、驻留因子、暴露剂量等。
(三)配方分析(仅针对于儿童产品)。
(四)配方中各成分的安全评估。包括产品中所有配方成分的标准中文名称、原料/成分在配方中的百分比、原料/成分风险评估情况等内容。
(五)可能存在的风险物质的安全评估。对产品可能含有的风险物质进行识别,并评估其安全性。
(六)安全评估结论。
(七)安全评估人员签名。
(八)安全评估人员简历。
(九)参考文献。
(十)附录
二、《产品配方整体安全分析》的证据类型
《产品配方整体安全分析》是依据不同证据类型,按照以下顺序依次对化妆品产品配方进行分析以确定其安全性。具体证据类型排序如下:
(一)《化妆品安全技术规范》中的限用组分、准用防腐剂、准用防晒剂、准用着色剂和准用染发剂列表中的原料。
(二)国内外权威机构[如世界卫生组织(WHO)、联合国粮农组织(FAO)、欧盟消费者安全科学委员会(SCCS)、美国化妆品原料评估委员会(CIR)等]已公布的安全限量或结论[如:化妆品安全使用结论、日允许摄入量、日耐受剂量、参考剂量、一般认为安全物质(GRAS)等]、国际日用香精协会(IFRA)已发布的香料原料标准等。
(三)原料历史使用浓度,是指原料在企业已上市(至少3年)的相同使用方法产品中的浓度。证明文件包括:1)国产特殊用途产品和进口产品递交的注册或备案配方(须与申报时提交配方一致);行政许可批件或备案凭证;以及产品上市证明文件;2)国产非特殊用途产品带原料含量或可计算原料含量的生产记录、工艺单、配料单;备案凭证;以及产品上市证明文件;3)不良反应监测情况说明。
(四)化妆品监管部门公布的原料最高历史使用量。
三、评估结论判定原则
(一)《化妆品安全技术规范》中有使用规定的原料,必须符合其使用要求。
(二)权威机构评估结论中所列的具有限制条件(如刺激性要求等)的原料,在采用该结论时应结合原料历史使用浓度、毒理学测试或人体临床测试结果,确保产品满足相应限制要求。
(三)只有系统毒性评估结论的原料,如一般认为安全物质(GRAS)原料、具有长期安全食用史的原料等,在采用该证据时应结合产品或原料历史使用浓度、毒理学测试结果或人体临床测试结果,对产品刺激性等局部毒性进行评估。
(四)同类产品配方中原料使用浓度应不高于原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量。
(五)同类产品配方中原料使用浓度高于产品原料历史使用浓度或化妆品监管部门公布的原料最高历史使用量,应按照《化妆品安全评估技术导则》进行安全评估证明其安全性。
(六)对于普通化妆品,不同类型产品的原料历史使用浓度可相互参考,暴露量高和接触时间长的产品,可用于暴露量低和接触时间短的产品评估,但需要从目标人群、使用部位和使用方式等方面充分说明其合理性。
(七)对于无法使用任一证据类型的原料和风险物质,应按照《化妆品安全评估技术导则》进行评估证明其安全性。
为促进我国化妆品行业安全评价能力的逐步提升,积极鼓励注册人、备案人严格依据《化妆品安全评估技术导则》进行产品的安全评估,形成《产品安全评估报告》